
|
Extra-calc v3.0
(сборка 3.0.5.2)
|

|
Extra-calc v3.0
(сборка 3.0.5.2)
|
Расчет склонности воды к солеотложению по РД 39-01478070-026ВНИИ-86, по Оддо-Томсону и РД 39-0147103-302-88Расчет склонности воды к солеотложению по РД 39-0148070-026ВНИИ-86 основан на использовании индекса насыщения (в РД он назван показателем стабильности) Стиффа-Дэвиса который равен разности рабочего рН и расчетного рНнас, соответствующего насыщению воды карбонатом кальция при заданных условиях. В методике по данному РД на основе измеренного рН определяется рабочий рН. Для расчета необходимо ввести: обводненность W, температуру рабочей среды во время отбора пробы t°раб, температуру при которой производятся измерения pHизм; измеренное значение pHизм; рабочее давление Рраб, давление при котором ведутся измерения Ризм, компонентный состав воды (концентрация компонентов в мг/л) и плотность раствора p. Результатом расчета является показатель стабильности (ПС), если ПС<=0, то вода является стабильной, т.е. отсутствует выпадение солей, если ПС>0, то вода склонна к солеотложению. 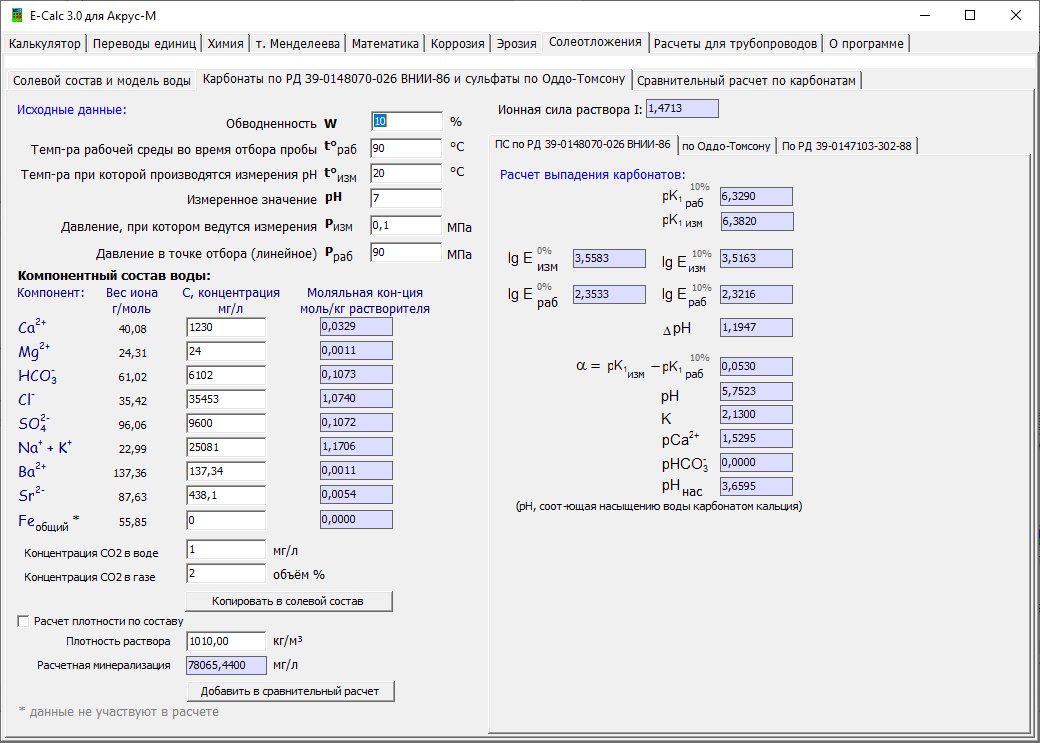
Расчет выпадения сульфатов производится по методике Оддо-ТомсонаМетод изложен В.Е. Кащавцевым, на основании зависимостей полученных Оддом и Томсоном. В нефтепромысловой практике прогнозные оценки солеотложения осуществляют-ся по степени насыщения вод солями, определяемой по формуле 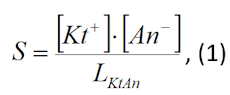
где [Kt+]·[An-] - произведение фактических концентраций солеобразующих катио-нов и анионов; LKtAn - термобарически равновесное произведение растворимости. При S>1 возможно выпадение солей, При S<1 в растворе содержится соединение в таком количестве, что осадок не выпа-дает. По методу Дж. Оддо и М Томсона оценку возможного выпадения сульфатных со-лей можно осуществлять по индексу насыщенности, определяемой по формуле 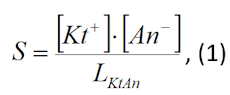
где при SI>0 предполагается выпадение солей, а при SI<0 – дефицит насыщенности раствора солевых соединений и отсутствие осадка. Относительно индекса насыщенности получена серия уравнений (табл. 1), которые могут использоваться в расчетах солеобразования. Таблица 1 - Уравнения по прогнозированию сульфат образующих солей
Примечание: [BaSO2+], [Sr2+], [Ca2+], [Mg2+], [HCO3-], [SO42-] – моляльные концентрации соответствующих ионов; Т – температура, oC; Р – давление, МПа; μ - ионная сила раство-ра определяется по формуле 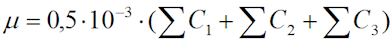
или 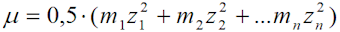
где Температурные диапазоны образования сульфатно-кальциевых отложений для различных модификаций солей неоднозначны. До температуры 80 oС преимущественно выпадает гипс, а после 120 oС сульфатно-кальциевый осадок полностью состоит из ангидрита. Диапазон температур 80-120 oС является переходным, в нем формируется бассанит, особенно в нетурбулентных системах, может встречаться любая из трех модифи-каций: вначале диапазона – гипс, в конце, после температуры 100 oС - главным образом ангидрит. В связи с этим соответствующие уравнения из таблицы 1 должны быть ориентированы на данный диапазон температур. 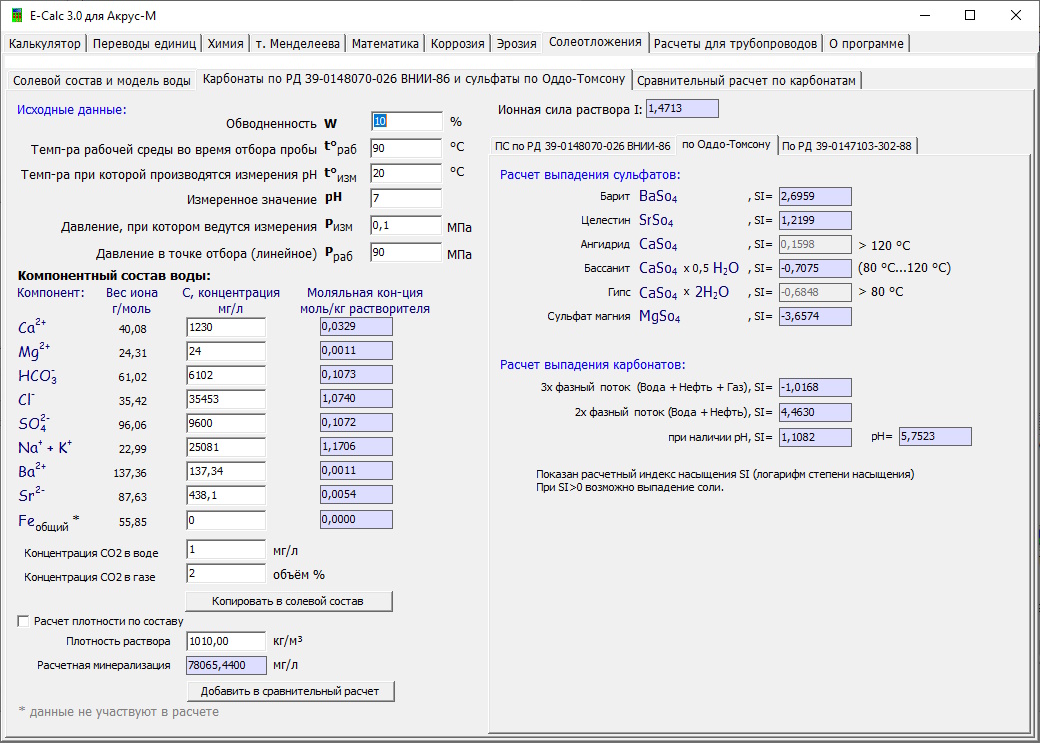
Метод оценки склонности нефтепромысловых вод к выделению твердых взвесей (осадка) сульфата кальция по РД 39-0147103-302-88Эта методика предназначена для оценки стабильности исследуемых водных сред в ши-роком интервале минерализации (пластовые, поверхностные воды, их смеси) к выделению твердого осадка сульфата кальция. Оценка производится расчетным путем на основании данных химического анализа ионного состава вод. Склонность исследуемой воды к выделению твердой взвеси (осадка) сульфата кальция CaSO4 рассчитывают по коэффициенту пересыщения SCaSO4 
где ПР - произведение растворимости сульфата кальция (принимается равным 3,05·10-5); ПА - произведение активности ионов; [Ca2+], [SO42-] - концентрации тех же ионов, моль/л; ƒCa2+, ƒSO42- - коэффициенты активностей соответствующих ионов. Из условия равенства зарядов ионов кальция и сульфата принимается равенство их коэффициентов активностей и среднего коэффициента активности для CaSO4. Коэффи-циенты активности находят по модифицированному уравнению Дебая Гюккеля: 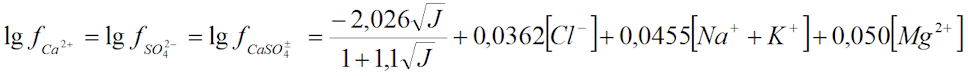
где [Cl-], [Mg2+], [Na+ + K+] - концентрация ионов, моль/л; J - ионная сила, моль/л. Ионная сила растворения солей в воде рассчитывается по формуле 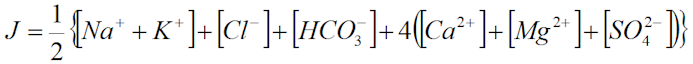
При степени насыщения SCaSO4 >1 принимается, что такая вода склонна к выделению твердой взвеси сульфата кальция. При необходимости количество выпадающего сульфата кальция рассчитывают по уравнению 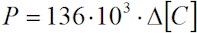
где P - количество выпадающего сульфата кальция, мг/л; 136 – молекулярная масса сульфата кальция, мг; 103 – переводной коэффициент; Δ[C] = [Cфакт] - [Cравн] - разность фактической и равновесной концентраций того из ионов, который по данным анализа находится в меньшем количестве. При [Ca2+] > [SO42-] - равновесная концентрация [SO42-]:
При [Ca2+] < [SO42-] - равновесная концентрация [Ca2+]:
Коэффициенты активности при этом ƒCaSO4± = ƒCa2+ = ƒSO42- 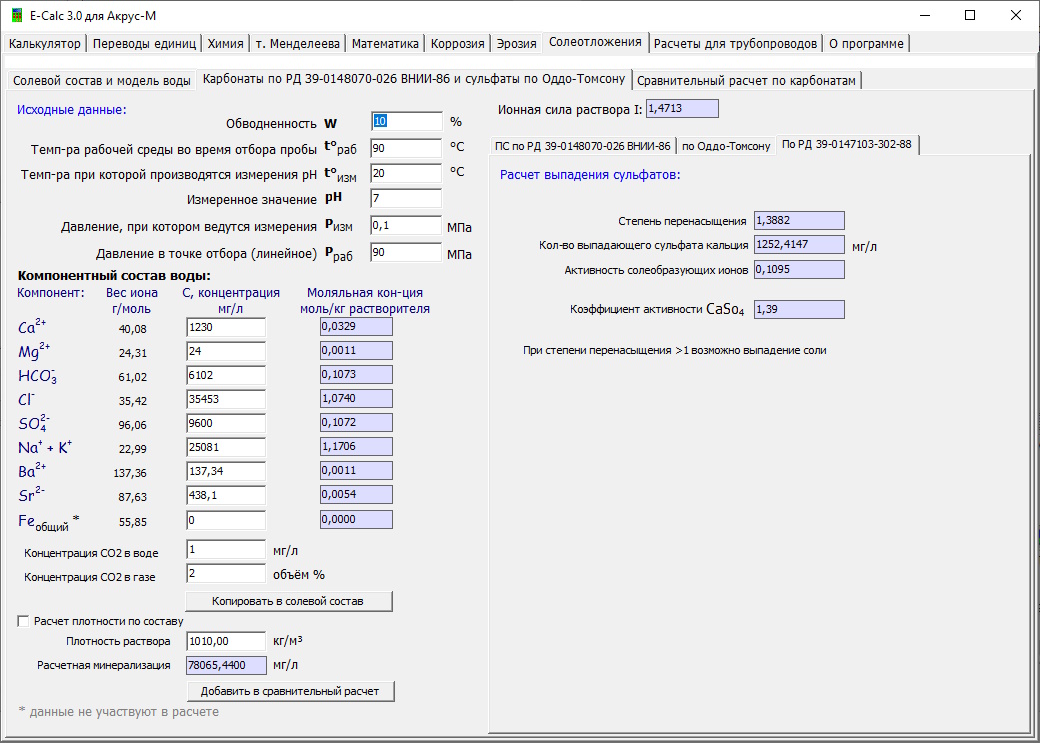
|